
ภาพฟีนอล์ฟทาลีน
อินดิเคเตอร์สำหรับกรด-เบส เป็นสารอินทรีย์ อาจเป็นกรดหรือเบสอ่อนๆ ซึ่งสามารถเปลี่ยนจากรูปหนึ่งไปเป็นอีกรูปหนึ่งได้ เมื่อ pH ของสารละลายเปลี่ยน
การเปลี่ยนสีของอินดิเคเตอร์
HIn เป็นสัญลักษณ์ของอินดิเคเตอร์ที่อยู่ในรูปกรด (Acid form)
In- เป็นสัญลักษณ์ของอินดิเคเตอร์ที่อยู่ในรูปเบส (Basic form)
รูปกรดและรูปเบสมีภาวะสมดุล เขียนแสดงได้ด้วยสมการ ดังนี้
In- เป็นสัญลักษณ์ของอินดิเคเตอร์ที่อยู่ในรูปเบส (Basic form)
รูปกรดและรูปเบสมีภาวะสมดุล เขียนแสดงได้ด้วยสมการ ดังนี้
HIn (aq) + H2O (l)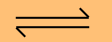 H3O+ (aq) + In- (aq)
H3O+ (aq) + In- (aq)
ไม่มีสี * สีชมพู* ; (* = กรณีเป็นฟีนอล์ฟทาลีน)
(รูปกรด) (รูปเบส)
ไม่มีสี * สีชมพู* ; (* = กรณีเป็นฟีนอล์ฟทาลีน)
(รูปกรด) (รูปเบส)
HIn และ In- มีสีต่างกันและปริมาณต่างกัน จึงทำให้สีของสารละลายเปลี่ยนแปลงได้ ถ้าปริมาณ HInมากก็จะมีสีของรูปกรด ถ้ามีปริมาณ In-มากก็จะมีสีของรูปเบส การที่จะมีปริมาณ HIn หรือ In มากกว่าหรือน้อยกว่านั้นขึ้นอยู่กับปริมาณ H3O+ ในสารละลาย ถ้ามี H3O+ มากก็จะรวมกับ In- ได้เป็น HIn ได้มากจะเห็นสารละลายใสไม่มีสีของ HIn แต่ถ้าอยู่ในสารละลายที่มี OH- มาก OH-จะทำปฏิกิริยากับ H3O+ ทำให้H3O+ ลดลง ซึ่งจะมีผลทำให้เกิดปฏิกิริยาไปข้างหน้าได้ In- มากขึ้น จะเห็นสารละลายในรูปของ In- คือเห็นเป็นสีชมพู
ช่วง pH ที่อินดิเคเตอร์เปลี่ยนสีจากรูปหนึ่งไปเป็นอีกรูปหนึ่ง สารละลายจะมีสีผสมระหว่างรูปกรดและรูปเบส เรียกว่า ช่วง pH ของอินดิเคเตอร์ (pH range หรือ pH interval)อินดิเคเตอร์และช่วงการเปลี่ยนแปลงตามค่า pH ที่ต่างกัน
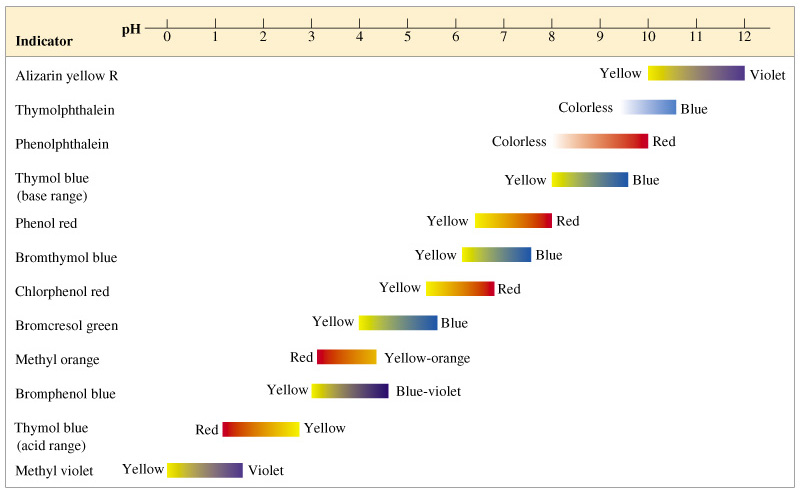
อย่างไรก็ตาม อินดิเคเตอร์ชนิดหนึ่งๆ จะใช้หาค่า pH ของสารละลายได้อย่างคร่าวๆ เท่านั้น เช่น เมื่อนำสารละลายมาเติม เมทิลออเรนจ์ลงไป (ช่วง pH ของเมทิลออเรนจ์เท่ากับ 3.0 - 4.4 และสีที่เปลี่ยนอยู่ในช่วง สีแดง  เหลือง) ถ้าสารละลายมีสีเหลืองหลังจากหยดเมทิลออเรนจ์ แสดงว่าสารละลายนี้มี pH ตั้งแต่ 4.4 ขึ้นไป ซึ่งอาจมีฤทธิ์เป็นกรด กลางหรือ เบส ก็ได้ ดังนั้น การหาค่า pH ของสารละลายหนึ่งๆ อาจจะต้องใช้อินดิเคเตอร์หลายๆ ตัว แล้วนำข้อมูลมาวิเคราะห์ pH ของสารละลายร่วมกัน
เหลือง) ถ้าสารละลายมีสีเหลืองหลังจากหยดเมทิลออเรนจ์ แสดงว่าสารละลายนี้มี pH ตั้งแต่ 4.4 ขึ้นไป ซึ่งอาจมีฤทธิ์เป็นกรด กลางหรือ เบส ก็ได้ ดังนั้น การหาค่า pH ของสารละลายหนึ่งๆ อาจจะต้องใช้อินดิเคเตอร์หลายๆ ตัว แล้วนำข้อมูลมาวิเคราะห์ pH ของสารละลายร่วมกัน
ยูนิเวอร์แซลอินดิเคเตอร์
สารละลายยูนิเวอร์แซลอินดิเคเตอร์ เป็นการนำอินดิเคเตอร์หลาย ๆชนิดที่มีการเปลี่ยนสีในช่วง pH ต่างกันมาผสมกันในสัดส่วนที่เหมาะสม จึงสามารถบอกค่าความเป็นกรด - เบส ของสารละลายโดยบอกค่า pH ที่ละเอียด และถูกต้องยิ่งขึ้น

อินดิเคเตอร์จากสารธรรมชาติ

อินดิเคเตอร์จากสารธรรมชาติ
นอกจากอินดิเคเตอร์กรด-เบส ที่เป็นสารอินทรีย์ที่กล่าวมาแล้ว ในธรรมชาติยังมีสารหลายชนิดที่มีสมบัติเหมาะสมที่จะใช้เป็นอินดิเคเตอร์ได้ พบว่าสารที่มีสีต่าง ๆ ซึ่งสามารถสกัดได้จากส่วนต่าง ๆ ของพืช เช่น ดอก ใบ
ตัวอย่างอินดิเคเตอร์ที่พบในธรรมชาติ
ชนิดพืช | สารที่ใช้สกัด | ช่วง pH ที่เปลี่ยนสี | สีที่เปลี่ยน |
อัญชัน ดาวเรือง ดาวเรือง หางนกยูง แคแดง ชงโค เข็มแดง เข็มแดง กระเจี๊ยบ คริสต์มาส คริสต์มาส บานไม่รู้โรย บานไม่รู้โรย แวนด้า ส้มเกลี้ยง(ผิว) สารภี สารภี ทองกวาว | น้ำ แอลกอฮอล์ น้ำ แอลกอฮอล์ น้ำ น้ำ น้ำ แอลกอฮอล์ น้ำ+แอลกอฮอล์+อีเทอร์ น้ำ แอลกอฮอล์+อีเทอร์ น้ำ แอลกอฮอล์ แอลกอฮอล์ น้ำ แอลกอฮอล์ น้ำ น้ำ | 1-32-3 11-12 10-11 2-3 10-11 4-5 6-7 6-7 6-7 7-8 5-6 6-7 6-7 5-6 8-9 6-7 8-9 10-12 10-11 3-4 | แดง - ม่วง ไม่มีสี - เหลืองอ่อน เหลือง - เหลืองน้ำตาล เขียว - เหลือง ชมพู - ส้ม ส้ม - เหลือง บานเย็น - แดง แดง - เขียว ชมพู - เขียว แดง - เหลือง เหลือง - เขียว ชมพู - เหลือง เหลือง - เขียว แดง - เขียว ชมพู - เขียวอ่อน เขียว - เขียวน้ำตาล แดง - ชมพู แดง - ม่วง ม่วง - น้ำเงิน ไม่มีสี - เหลือง |
ไม่มีความคิดเห็น:
แสดงความคิดเห็น